放弃对160品种开展一致性评价,是明智之举还是无奈?
时间:2017-08-28 来源: E药经理人
近日,浙江省食药监局发布《浙江省拟不开展仿制药质量和疗效一致性评价的品种信息》,其中共32家药企的160个药品计划拟不再开展仿制药一致性评价。
对于大多数药企而言,一致性评价工作时间紧、评价费用昂贵,因此对手中所有品种均开展一致性评价很难实现,而这160个品种被这些企业放弃,则意味着这项工作开展一年多来,各企业对自身工作面临的形势和推进程度有了更加清晰的认识,也做出了更加现实的决定。
国泰君安证券分析指出,按照2018年底大限,中小企业度选择放弃相关品种,节省时间和资金用于进展较快、最有希望争夺市场品种上,不失为明智之举。
与此同时,这160个被制药企业拟放弃开展一致性评价的品种一定是经过企业管理层权衡、评估、综合考虑后的结果。这是目前全国第一个省份统一公布拟放弃名单,其他省份或会跟进,这种方式方便企业更为理性筛选品种,也有利于企业理性做出选择, 并在整体上加快仿制药一致性评价的进展。
1、药企:有的放弃大半品种
整体来看,涉及拟放弃品种目录的企业数量有32家之多,其中普洛药业旗下的浙江巨泰制药有限公司是申报拟放弃品种数最多的公司,共计35个品种。而申报拟放弃品种数大于等于5的制药企业共有12家,按照上市公司子公司归并后,康恩贝、三生制药、新光药业、海正药业、华海药业等上市公司均有较多品种宣布拟放弃一致性评价。
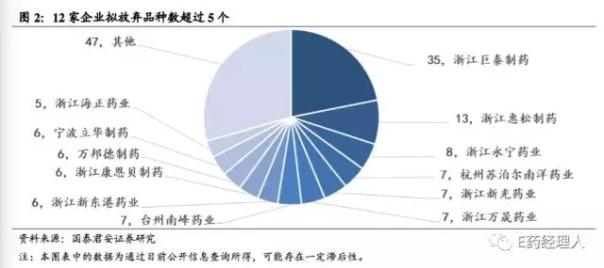
甚至有的企业拟放弃的品种数量已经占全书品种数量的一大半。以普洛药业为例,其旗下子公司浙江巨泰制药有限公司截至2017年7月底共获得41个品种的“国药准字”批文,而此次直接拟放弃其中35个品种的一致评价工作,只保留了头孢克肟分散片、阿莫西林克拉维酸 钾胶囊(2个规格)、灭菌结晶磺胺、维生素E烟酸酯等品种。据悉,头孢克肟分散片、阿莫西林克拉维酸钾胶囊是普洛药业的主要产品, 其市场份额在2017年上半年保持稳健提升,目前已备案参比制剂,BE试验即将启动。
再以新光药业为例,此次拟放弃7种化学药的一致性评价工作。据了解,该公司主打中成药业务,公司主导产品黄芪生脉饮、伸筋丹胶囊和西洋参口服液2016年合计营收占总营收比高达98.5%。因此,行业预计拟放弃7种化学药的一致性评价对公司未来业绩影响整体较小。
国泰君安证券分析指出,从目前一致性评价的进展来看,BE试验走在前列的主要为石药集团、上海医药、联邦制药等具备充裕资金和雄厚研发实力的大型医药企业,中小型制药企业度自身无力与之竞争相关品种,选择直接放弃,节省资金用于自身进展较快、最有希望抢占市场的品种的一致性评价工作,较为明智。
2、品种:舍“小”保“大”
从被放弃的品种来看,整体浙江省公布的拟被放弃的品种的共同点在于:竞争激烈且品种是这些企业的非核心品种。据国泰君安证券研究报告分析,这160个拟放弃品种现有批文数目众多,竞争激烈,绝大部分在中检所已有较多企业进行过参比制剂备案。
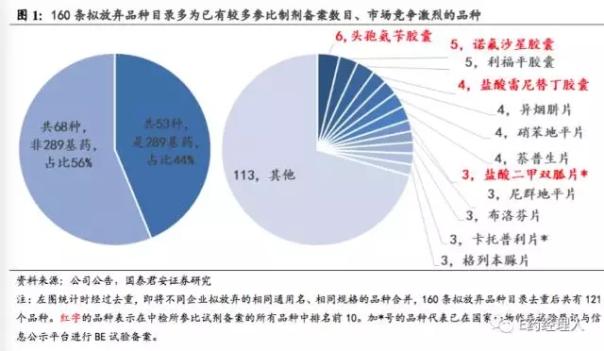
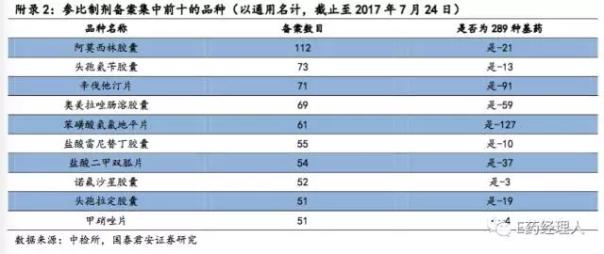
如头孢氨苄胶囊(以通用名计)就有5家企业宣布拟放弃一致性评价。头孢氨苄胶囊是首批“289”目录中的基药之一,同时也是中检院公布的参比制剂备案数目总排名第2的品种。同时,诺氟沙星胶囊、盐酸雷尼替丁胶囊、盐酸二甲双胍片等被多家企业放弃的品种也位居中检院公布的参比制剂备案数总排名前10名。据悉,以上四个品种已有批文数目均超过100,且生产企业数量多,竞争激烈。
此外,还有阿莫西林胶囊、盐酸二甲双胍片等品种已有石药集团、复星医药等大型医药企业完成全部BE试验。
数据显示,截止至2017年7月24日,中检所共公开629家仿制药企业备案的约4000个参比制剂备案条目,其中涉及到289个基药目录的有2294个,占比57%;289个基药品种中的223个已有企业备案参比制剂,占比77%。截止2017年8月4日,160条拟放弃品种目录(去重后是121个品种)中目前已进行BE试验备案的约有5种,分别是:阿莫西林胶囊、 阿奇霉素胶囊、盐酸二甲双胍片、盐酸克林霉素胶囊、卡托普利片, 除卡托普利片外,其余4种品种均有BE试验已经完成。
根据2016年3月国务院办公厅印发的《关于开展仿制药质量和疗效一致性评价的意见》要求:“国家基药品种中,在2007年10月1日前批准上市的化学药品仿制药口服固体制剂,应在2018年底前完成一致性评价,逾期未完成的,不予再注册”。以及,“同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种”。
因此,这些企业放弃这些品种的评价工作,也就意味着其文号将被注销,企业将不能再销售该品种,失去该品种目前的市场份额。但是这批拟被放弃品种均为各家上市公司的非核心品种,且这些品种的销售占企业收入比例较低,分析认为长期来看企业选择放弃对未来销售收入影响整体较小。
3、未来:“剩”者为王
一致性评价进行至今,无论是监管部门还是企业自身都对这项改革任务的重要性有了清晰和深刻的认识,也越来越秉持开放时效的态度,未来一年将是一致性评价的关键期,预计陆续将有品种通过一致性评价,中国制药工业的洗牌正式开始。
6月28日,浙江省食药监局发布公告称,已经完成了对浙江京新药业股份有限公司的瑞舒伐他汀钙片仿制药一致性评价的初审工作并上报国家总局。紧接着,江苏省泰州市食药监局发布的文章《省食药监局大力推进仿制药质量和疗效一致性评价工作》称,截至6月中旬,江苏省已有扬子江药业集团等4家企业6个品规完成一致性评价,并向省局申报。如今,浙江省再次公布相关进展,可谓是走在了改革的最前方。
国泰君安证券指出,随着一致性评价的推进,中国化学制药产业去产能化、“剩”者为王、优化市场竞争格局的供给侧改革的春天将到来,制药行业进入长周期新起点。尤其是工业基础扎实、有一定的利润体量、品种数量较多、重视一致性评价,且评价进展顺利的优秀治疗型品种制药企业最终会受益于行业变局的结构性机会。
虽然短期来看,不进行一致性评价的品种将逐渐退出市场,企业将面临销售品种减小所带来的利润下行风险。然而,如能利用拟放弃各自的非优势品种的一致性评价工作节省下来的物力和财力快速推进自身核心优势品种的一致性评价工作,争取尽早通过,则有望抢占新的市场份额,实现弯道超车。
一致性评价工作持续推进,品种压缩早已经是行业趋势,淘汰掉小品种后剩下的将是各制药企业最具代表性的大品种,拥有优秀品种的制药企业最终会受益于行业变局。虽然仿制药一致性评价的威力可能暂时还未真正发挥出来,但是随着越来越多的品种完成评价,留给很多企业的时间真的不多了!
